发布日期:2025-06-12
肺癌,这个在我国乃至全球都令人闻之色变的“健康杀手”,长期霸占着发病率和病死率的榜首。尽管靶向与免疫治疗等现代医学手段给患者带来了新希望,但术后复发与远处转移仍是制约长期生存率的关键因素,也成为每一位肺癌患者心中最深的恐惧。


在肺癌治疗领域,微小病灶残留(MRD)逐渐走入人们的视野。大量研究表明[1],基于循环肿瘤DNA(ctDNA)的MRD比传统的肿瘤标志物或影像学方法更具优势,能更早鉴定出肺癌患者术后复发的迹象,更早识别复发高风险患者,为提前干预创造宝贵机会,在肺癌患者的预后预测、复发风险评估及辅助治疗指导等方面发挥着举足轻重的作用。
目前,基于NGS的ctDNA突变检测,是当下实体瘤MRD检测的常用方法。但不得不说,MRD监测的价格并不亲民。市场上主流的MRD监测套餐,多为1+n,需在两年内完成,这样一套下来价格万元级别。若再增加监测次数,费用还会水涨船高,这无疑给患者和家属带来了沉重的经济负担。因此,如何实现术后患者高灵敏、低成本且动态化的MRD监测,至今仍是精准医学领域亟待攻克的核心难题。
在此背景下,基于数字PCR(dPCR)联合NGS对原发肿瘤患者的常见驱动基因ctDNA进行MRD复发监测逐渐成为一种可行性方法。尽管目前有多种NGS的Panel可供选择,但由于很多基因或者位点的临床意义不明确而被排除。非小细胞肺癌(NSCLC)占全部肺癌85%[2],而表皮生长因子受体(EGFR)在NSCLC治疗中是极为关键的靶点。相关研究表明,dPCR为携带常见驱动基因(如EGFR)的手术切除NSCLC患者的MRD检测提供了一条可行路径,其准确性也得到了相关分析结果的有力支撑。

《实体瘤分子残留病灶检测共识(2024年)》指出,基于NGS的MRD检测因高通量、全面性和高灵敏度,成为当下主流。不过,基于dPCR的MRD个性化定制,能对低丰度ctDNA进行精准绝对定量,同样具有独特价值。

2024年《肺癌适应性治疗中国专家共识》[3]首次推荐ctDNA-MRD作为适应性治疗的标志物,阳性可指导升阶治疗,阴性可考虑降阶治疗。EGFR突变阳性NSCLC完全性切除术后MRD阴性患者,可考虑降阶辅助治疗;EGFR突变Ⅳ期NSCLC经过系统和局部治疗后,影像学无可见或无代谢肿瘤病灶时,可在生物标志物指导下考虑药物假期。

《非小细胞肺癌分子残留病灶专家共识(2021年)》[4]中提及,在一项前瞻性多中心研究里,共纳入101例带有体细胞突变的早期乳腺癌患者,通过dPCR动态追踪术后血浆ctDNA,结果清晰地表明ctDNA阳性与患者疾病复发密切相关,且ctDNA较影像学可提前预示疾病复发,中位时间达10.7个月。

在一项综合FLAURA与AURA3研究的探索分析中[5],通过dPCR检测基线血及治疗后3/6周血的EGFR突变状态,发现基线血阴性患者预后均较阳性者好,其次,基线血阳性患者若治疗后3周达到ctDNA清零状态预后较未清零者好(AURA3奥希替尼组:10.9个月vs. 5.7个月;FLAURA奥希替尼组:19.8个月vs. 11.3个月)。
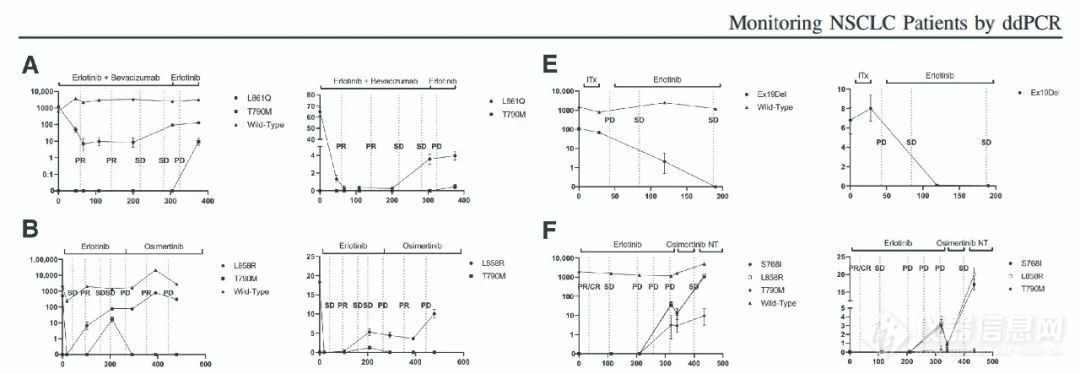
一项研究[6]对6名NSCLC患者分析了监测数据,dPCR结果很好地反映了疾病的进程和放射学反应。证实了dPCR多重检测能够纵向监测液体活检中的EGFR突变状态,ctDNA浓度和突变丰度(FA)的变化反映了治疗反应,与病程一致;因此,它可能是晚期NSCLC患者个性化治疗管理中有用的监测工具,对监测EGFR酪氨酸激酶抑制剂治疗具有重要意义。
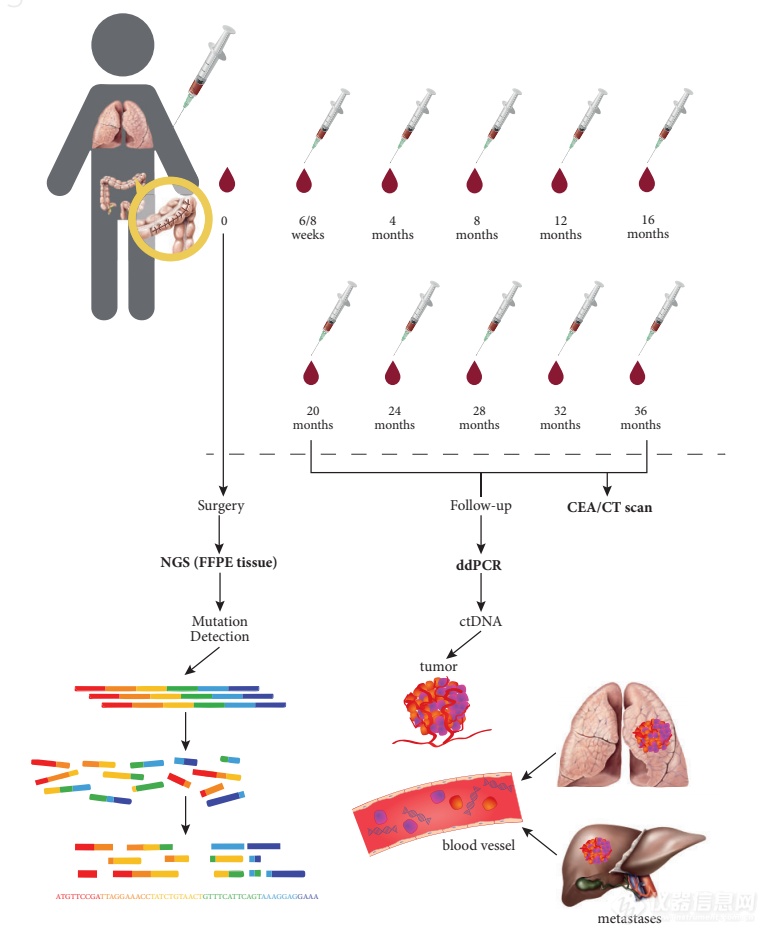
在这项研究中[7],选取了150名被诊断为局部结直肠癌患者,定制靶向的29基因NGS panel检测原发性肿瘤突变。选择突变频率高的突变位点,再使用dPCR对血液中的ctDNA进行监测,并跟踪临床的复发情况。结果显示手术后和随访期间在血浆样品中检测到ctDNA的无病生存期(DFS)较差。在接受辅助化疗的患者中,治疗后ctDNA的存在与早期复发相关。在对ctDNA进行监测可比影像学提前11.5月提示复发。
基于这些应用研究,NGS与数字PCR的组合应用,为实现肿瘤MRD更精准、更具成本效益且具有时效性的检测带来了新希望。在MRD检测中,通过NGS测序识别个体特异突变位点,筛选高频突变作为dPCR追踪目标,指导dPCR针对特定基因突变进行高灵敏度检测;dPCR则能对MRD进行定量分析,精确计算ctDNA拷贝数变化,直接提供突变率,更好地评估治疗效果、预测复发风险和判断疾病预后。相比动辄上万的MRD方案,dPCR定向追踪特定基因实时监测的方案,目标明确,性价比更高。
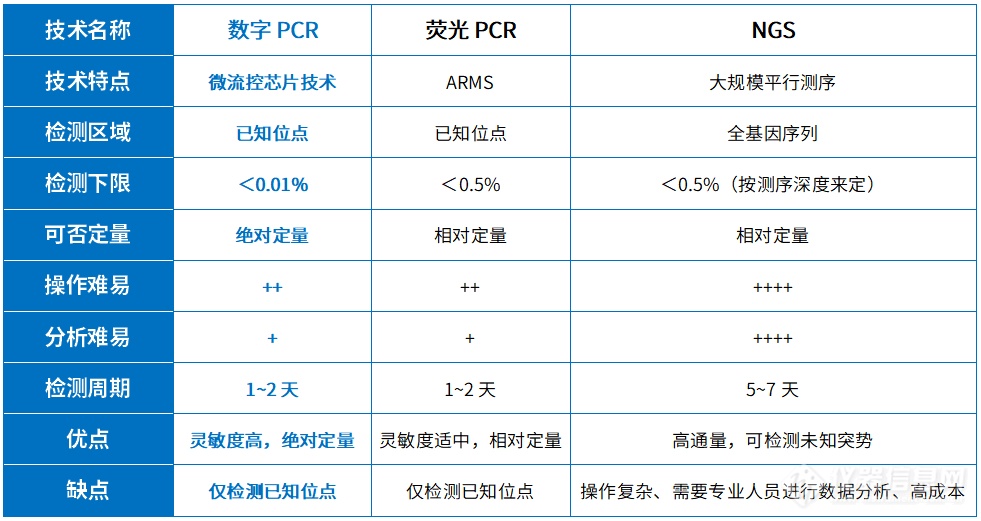


新羿生物dPCR具备了本地化落地门槛低,运营成本低,实验操作容易,报告出具快的特点,可以充分发挥dPCR检测速度快,灵敏度高,可绝对定量,能够获得突变丰度信息的优势,非常适合于低丰度ctDNA持续动态低成本监测。临床研究证实了dPCR技术用于肺癌检测的可行性和优越性,为开发基于NGS-dPCR联用的肺癌MRD监测新策略筑牢了基础。
数字PCR在肺癌MRD监测领域展现出巨大的潜力,有望成为临床医生手中更精准、更经济、更便捷的监测利器,为肺癌患者的治疗与康复带来更多曙光。
参考文献:
[1]. 中华医学会病理学分会,国家病理质控中心. 实体瘤分子残留病灶检测共识[J]. 中华病理学杂志, 2024, 53(11): 1088-1096.
[2]. 国家卫生健康委办公厅. 原发性肺癌诊疗指南(2022年版)[J]. 协和医学杂志, 2022, 13(4): 549-570.
[3]. 吴一龙,陆舜,程颖,等.肺癌适应性治疗中国专家共识[J]. 循证医学, 2024, 24(4): 193-200.
[4]. 吴一龙,陆舜,程颖,等.非小细胞肺癌分子残留病灶专家共识[J]. 循证医学, 2021, 21(3): 129-135.
[5]. Gray JE, Ahn MJ, Oxnard GR, et al. Early Clearance of Plasma Epidermal Growth Factor Receptor Mutations as a Predictor of Outcome on Osimertinib in Advanced Non-Small Cell Lung Cancer; Exploratory Analysis from AURA3 and FLAURA. Clin Cancer Res, 2023, 29(17): 3340-3351.
[6]. De Kock R, Van Den Borne B, Youssef-El Soud M, et al. Therapy Monitoring of EGFR-Positive Non-Small-Cell Lung Cancer Patients Using ddPCR Multiplex Assays. J Mol Diagn, 2021, 23(4): 495-505.
[7]. Tarazona N, Gimeno-Valiente F, Gambardella V, et al. Targeted Next-generation Sequencing of Circulating-tumor DNA for Tracking Minimal Residual Disease in Localized Colon Cancer. Ann Oncol, 2019, 30(11):1804-1812.
●关于新羿生物●
新羿生物成立于2015年,位于中关村科技园,是国家高新技术企业、北京市“专精特新”企业,专注于生命科学与分子诊断的自主创新,拥有在仪器、芯片、材料、试剂、软件等领域的高水平研发团队。公司发展迅速,申请国内外专利200余项、授权专利150余项,持续在权威期刊发表学术论文,承担国家级科研基金。公司基于自主知识产权的数字PCR技术,已获得首个及第二个共三项数字PCR仪NMPA III类医疗器械注册证,三项诊断试剂NMPA III类医疗器械注册证,其中感染和实体瘤液体活检领域均为首个数字PCR诊断试剂III类注册证,两次获得中国体外诊断优秀创新产品金奖,荣获中关村国际前沿科技创新大赛总冠军,荣获北京市科学技术二等奖。公司自主研发的开放式分子POCT一体机及qPCR快检试剂均获NMPA III类医疗器械注册证。公司秉承“创新,让精准触手可及”的理念,发展多指标、高通量、自动化、防污染、成本低的先进技术,致力于成为领先的生命科学和分子诊断企业,服务于生命科学、精准医疗、药物开发及健康管理。


京公网安备 11010802028168号